Sự khác biệt chính: Liên kết ion là liên kết hóa học giữa hai nguyên tử khác nhau (tức là kim loại và phi kim) trong đó một nguyên tử nhường electron cho một nguyên tử khác. Một liên kết cộng hóa trị là một liên kết hóa học mạnh khác. Nó diễn ra là các nguyên tử tương tự (tức là hai phi kim). Trong liên kết cộng hóa trị, hai nguyên tử kết hợp với nhau để chia sẻ electron, thay vì một nguyên tử lấy electron từ người khác.
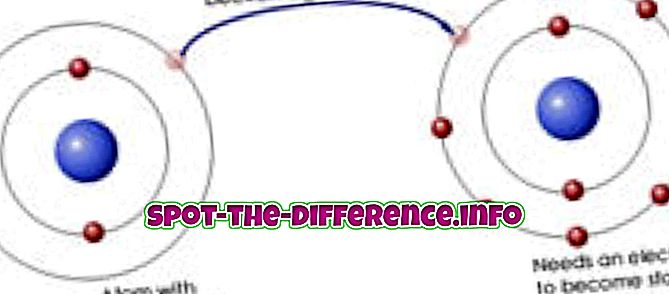
Liên kết ion là liên kết hóa học giữa hai nguyên tử khác nhau (tức là kim loại và phi kim) trong đó một nguyên tử nhường electron cho một nguyên tử khác. Do đó cả hai nguyên tử trở thành các ion vì một nguyên tử có ít hơn một electron, trong khi nguyên tử kia có thêm một nguyên tử. Các ion kim loại bị mất một điện tử có điện tích dương. Các ion phi kim loại thu được một electron có điện tích âm. Khi các mặt đối lập thu hút, các ion này sau đó bị hút mạnh vào nhau, mạnh đến mức chúng trở nên liên kết.
Các hợp chất ion thường ở dạng chất rắn, tức là muối. Chúng hòa tan cao trong nước và có điểm nóng chảy cao. Khi chúng ở trong nước, chúng cũng có độ dẫn điện cao.

Liên kết cộng hóa trị bao gồm nhiều loại tương tác, bao gồm liên kết, liên kết π, liên kết kim loại với kim loại, tương tác không tin và liên kết hai electron hai tâm. Khi một nguyên tử có một electron ở lớp vỏ ngoài của nó và một nguyên tử khác yêu cầu một electron để lấp đầy lớp vỏ ngoài của nó, hai nguyên tử này cùng nhau để chia sẻ electron. Do đó, cả hai nguyên tử cuối cùng đều có vỏ ngoài đầy đủ và tương ứng là cấu hình điện tử ổn định.
Liên kết hóa học được tạo ra để nguyên tử có thể có vỏ ngoài đầy đủ, vì vỏ ngoài đầy đủ có nghĩa là cấu hình điện tử ổn định. Trong liên kết ion, khi nguyên tử kim loại có một electron ở lớp vỏ ngoài và phi kim cần một electron để hoàn thành lớp vỏ ngoài của nó, nguyên tử kim loại đưa electron của nó cho phi kim. Tương tự, trong liên kết cộng hóa trị, chúng chia sẻ electron bằng nhau.
Sự gắn kết | Liên kết cộng hóa trị | |
Định nghĩa | Một liên kết hóa học giữa hai nguyên tử khác nhau trong đó nguyên tử nhường một electron cho một nguyên tử khác. | Liên kết cộng hóa trị là liên kết hóa học liên quan đến việc chia sẻ các electron giữa hai nguyên tử tương tự nhau. |
Xảy ra | Một kim loại và một phi kim loại | Hai phi kim |
Cực tính | Cao | Thấp |
Hình dạng của phân tử | Không có hình dạng nhất định, cấu trúc mạng | Hình dạng cụ thể |
Tinh dân điện | Cao | Thường không có |
Dẫn nhiệt | Cao | Thường thấp |
Điểm nóng chảy của chất | Khác nhau, nhưng thường cao hơn các hợp chất cộng hóa trị | Khác nhau, nhưng thường thấp hơn các hợp chất ion |
Điểm sôi của chất | Cao | Khác nhau, nhưng thường thấp hơn các hợp chất ion |
độ hòa tan trong nước | Cao | Khác nhau, nhưng thường thấp hơn các hợp chất ion |
Trạng thái của chất ở nhiệt độ phòng | Thường rắn | Chất rắn, lỏng, khí |